コロナウイルス 抗体検査キット、日本国内で診断薬承認を目指す
支援総額
目標金額 3,000,000円
- 支援者
- 9人
- 募集終了日
- 2020年6月30日

Kansaiわんスリーサポーター!~盲導犬の育成にご支援を~
#医療・福祉
- 総計
- 39人

全国の身体障がい者に介助犬を届けたい|マンスリーサポーター募集中!
#医療・福祉
- 総計
- 47人

台湾花蓮地震 緊急支援
#国際協力
- 現在
- 47,377,000円
- 寄付者
- 4,858人
- 残り
- 73日

夜の世界で孤立・困窮している女性たちに、必要な支援を届けたい
#医療・福祉
- 総計
- 199人

車いすユーザーの社会参加を応援する!WheeLog!サポーター
#観光
- 総計
- 136人

脳腫瘍と闘う子どもたちへ、遺伝子検査を届ける研究を継続したい!
#子ども・教育
- 現在
- 4,715,000円
- 寄付者
- 328人
- 残り
- 8日

ファシリティドッグ ドリーム☆サポーターを募集中!
#子ども・教育
- 総計
- 180人
プロジェクト本文
<プロジェクト概要>
・新型コロナウィルスに対する抗体(IgMおよびIgG)を測定するイムノクロマト法の測定試薬の日本国内での診断薬承認を目指します。
・キットは中国の診断薬メーカー INNOVITA (TANGSHAN) Biological Technology Co.,Ltd. 社が製造する「COVID-19 IgG/IgMイムノクロマトキット」で、中国において体外診断用医薬品として利用されている製品です。
・イムノクロマト法はインフルエンザ検査等でよく利用されている迅速測定法。PCR法に比べて迅速・簡便で、少量の血液を使って、15分間で結果判定ができるという利点があります。
<資金の使い道>
・目標金額300万円は、第2フェーズの「診断薬としての使い方の開発」に関する研究測定にかかる費用に充当させていただきます。
・2020年9月中に研究測定を完了し、必要な結果が得られた場合は、その後診断薬承認のための研究、申請を行い、順調にいけば2022年の診断薬承認を予定しています。
※本プロジェクトは、抗体検査が診断薬になることを保証するものではありません。診断薬化に向けて必要な研究開発を行い、その結果として再度測定方法の開発が必要になる可能性もあります。
■プロジェクトに関するQA
Q:新型コロナウイルスの検査方法について、違いを教えてください。
A:

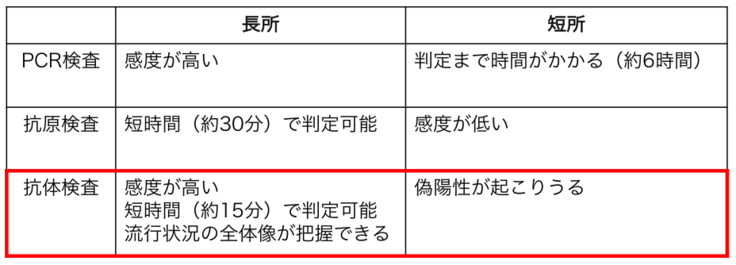
Q:これらの検査方法は、どのように使い分けられているのでしょうか?
A:現在のところ、明らかになっておらず、それを確定するための研究を計画しているというのが実情です。
抗体検査の役割は、PCR検査や抗原検査では見つけられない患者を一人でも多く見つけ出すことです。
現在は、HIVやC型肝炎で抗体検査と抗原検査が併用されています。
*実際の臨床現場の流れとして、以下の流れが考えられ、検証を進めていく予定です。
1. 疑われる症状がでている患者が来院
2. 抗原検査を実施(インフルエンザなどの検査で除外診断も行う)
3. 抗原検査陰性でも疑われる場合、抗体検査+PCR検査
4-1. PCR検査陽性なら治療。PCR検査陰性かつ抗体検査陽性なら経過観察、CT検査
4-2. PCR検査陰性、抗体検査陰性なら経過観察
Q:今回のプロジェクトの研究では、「抗体検査を使用する理由」を明らかにするとのことですが、具体的にどのような仮説があるのかを教えてください。
A:抗体検査の使い方として、現在以下の4通りが考えられます。これらの使い方の仮説を明らかにするために研究を行います。4の重症度予測とは、今後コロナウイルスに感染した場合に、重症化する可能性を判別します。

Q:ウィズコロナ時代における、抗体検査の役割を教えてください。
A:抗体検査は、PCR検査で偽陰性の患者を見つけ出せる可能性があるため、PCR検査や抗原検査を補完する検査として使用することができます。血液検査なので検体採取のリスクも低く、短時間で結果判定ができるため、幅広く検査を実施することができますので、無症状患者の発見にも役立ちます。
また、ワクチン接種が一般化した後には、摂取後の抗体の有無を確認することができます。
PCR検査の弱点を補う可能性のある抗体検査の診断薬承認を目指す
はじめまして。株式会社TKResearch 稲垣貴之です。私たちは、体外診断用医薬品(診断薬)の研究開発を行っているバイオベンチャーで、2020年5月で設立4年目を迎えます。
私たちは「研究成果をいちはやく臨床現場に届けたい」という想いのもと、さまざまな研究機関や国内外のメーカー・大学と共同研究開発を進めています。
新型コロナウイルス感染症は、現在では世界中に感染が拡大し、日本も例外ではなく、4月に緊急事態宣言が発令され、外出自粛の中、国民全員が感染の不安と闘っています。
そのような状況下で私たちは、私たちのホームグラウンドである「診断薬」というフィールドで、新型コロナウイルス感染症対策に協力したいという想いから、3月11日より、私たちの共同開発先である中国の診断薬メーカー INNOVITA (TANGSHAN) Biological Technology Co.,Ltd. 社が製造する抗体検査キットの輸入販売を開始しました。
彼らは中国・欧州でこの抗体検査キットを診断薬としての承認である「CFDA承認(中国)」「CEマーク(欧州)」を得て販売しています。
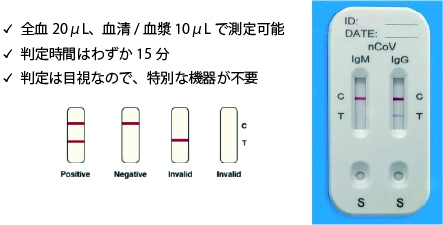

この抗体検査はイムノクロマト法という測定原理で、インフルエンザ検査等でよく利用されている迅速測定法です。少量の血液を使って、15分間で結果判定ができるという利点があります。PCR法に比べて迅速・簡便で、検体採取時の医師の感染リスクも大幅に低減できると考えられています。
しかしながら、PCR法と同等の検査結果を得られる検査方法ではなく、詳細については、ページ内の章「新型コロナウイルスの従来の検査手法(PCR法)と抗体検査の違い」をご覧ください。
私たちは、この抗体検査キットを、1箱20回入りで55,000円(税込)の価格で研究用試薬として医療機関に対して既に販売しています*1。つまり、1回の測定で必要なキット代金が2,750円(税込)と比較的安価な製品です。現在、北海道~九州まで日本全国の大学病院・医療機関・研究機関から注文を受け、キットを提供していますので、国内の複数の機関において研究が始まっています。
(*1 株式会社TKResearch、「COVID-19 IgG/IgMイムノクロマトキット」受注開始)
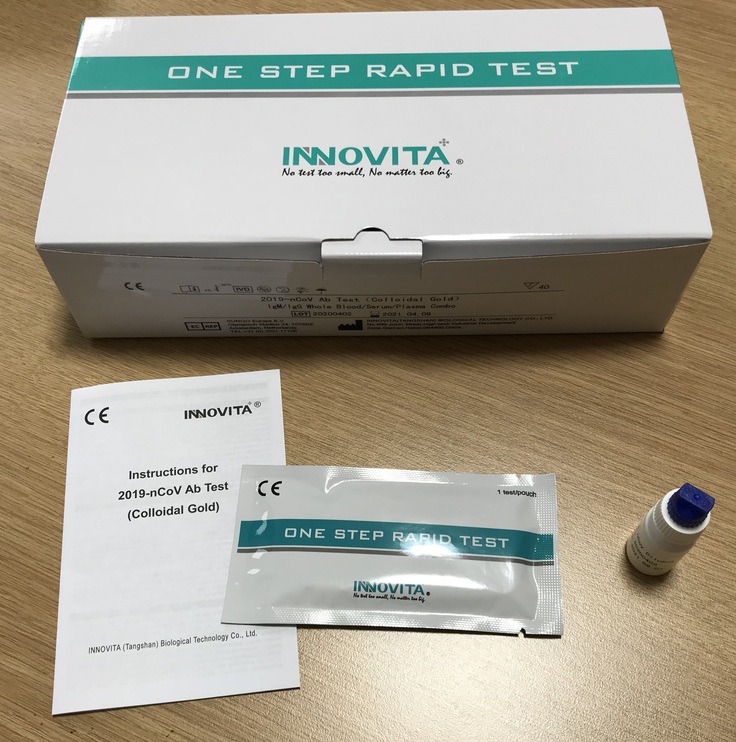
※本製品は研究用試薬です。現時点では、医薬品医療機器法に基づく体外診断薬用医薬品として承認・認証等を受けておらず、日本国内では診断目的では使用できません。また、医療機関向けの販売のため、個人の方等への販売はございません。
私たちが最終的に目指すのは、この抗体検査キットを日本国内で診断薬として厚生労働省より承認を受け、保険診療の範囲内で使用できるようにすることです。そしてPCR法とともに、互いを補完し合うような形で使用していただくことです。
そのためには、
①抗体検査を使用する理由、②結果の解釈方法、③結果の解釈
を受けて、次に行う治療や診断の方向性を示すことが必要になります。
私たちは、この抗体検査キットの存在を広めながら、まずは「①抗体検査を使用する理由」を明らかにしていく研究をしたいと考えています。そのためには、研究に使用するイムノクロマトキット【1000テスト分(50セット)】を調達する必要があります。
<研究のスケジュール>
■第1フェーズ
⓪キットの開発(INNOVITA社により済)
■第2フェーズ
①イムノクロマトキット購入(2020年6月まで)
②(診断薬ではなく研究試薬として)国内の医療機関など10施設を目途に提供(2020年7月まで)
③約5施設よりおよそ500件の検査キットの調査データ(1.各抗体の陽性率、2.可能な場合は、抗体陽性患者のPCR検査結果、CT検査での異常の有無、3.実際の使用状況)を収集して調査結果にまとめる(2020年9月まで)
■第3フェーズ
④診断薬として申請するための試験を実施する(2021年予定、診断薬メーカーと医療機関にて実施)
⑤申請するためのデータとして書類を揃える(2021年予定、診断薬メーカーにて実施)
⑥厚労省に申請を行う(2021年以降を予定、診断薬メーカーにて実施)
⑦厚労省による承認(通常承認までに1年程度、2021年末~2022年予定)
※結果次第で、①〜③を繰り返し行い、承認を得られるまで継続しますが、本クラウドファンディングの第一目標でご支援いただいた資金で実施するのは、①〜③までです。
※本プロジェクトは、抗体検査が診断薬になることを保証するものではありません。診断薬化に向けて必要な研究開発を行い、その結果として再度測定方法の開発が必要になる可能性もあります。
研究を行い、診断薬の承認を目指すためには、みなさまのご支援が必要です。ぜひご協力をお願いいたします。
現在、新型コロナウイルスの確定診断では「PCR法」という検査手法が用いられています。PCR法は、ウイルスのRNAを検出するので、ウイルスが現在体内に存在するかどうかを直接検出することができますが、死んだウイルスのRNAも検出できてしまうので、今現在感染力があるウイルスが体内に存在するかどうかまでは判断できません。
一方、抗体検査では、現在患者体内にウイルスが存在しているのかどうかは判定できませんが、IgM抗体とIgG抗体をそれぞれ検出することで、感染状態(感染初期なのか、急性期なのかなど)を判断できる可能性が指摘されています。
また、血液検査という一般的な方法であり、1検体の検査に15分(PCR法は4~6時間)と簡便に測定できることから、中国国内ではPCR陰性患者の経過観察や、治療中の患者の継続観察に使用されています。
このような観点から、抗体検査は単独で実施する検査ではなく、PCR法とともに使用していくことが望ましいと考えています。
抗体検査の原理と使用方法
現在世界中のメーカーが抗体検査を開発を進めており、多数の製品が発売されていますが、その原理はほぼ同様で以下の通りです。
<イムノクロマト法の測定原理>
NNOVITA社のイムノクロマトキットでは、以下の図のような原理で構成されており、これにプラスチックケースを被せて製品化しています。
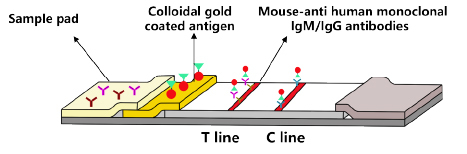
検出を行う部分にはニトロセルロース膜が使用され、膜の上に、抗ヒトIgMマウス抗体もしくは抗ヒトIgGマウス抗体(Tライン上)、抗マウスIgGヤギ抗体(Cライン上)が固相化されています。また、検出に使う金コロイド粒子には、リコンビナント抗原とマウスIgG抗体が固相化されています。
イムノクロマトキットに添加した検体は、まずサンプルパッドに染み込み、右側に移動していきます。その途中で、検体中の新型コロナウィルス抗体が金コロイド上のリコンビナント抗原に結合していきます。検体溶液は毛細管現象で徐々に右側に移動していき、その過程で、新型コロナウィルス抗体が結合した金コロイド粒子はTライン上に集まり、紫色のラインが肉眼で検出できます。また、抗体が結合しなかった金コロイドはCライン上に集まり、紫色のラインが発生します。
非常に多くの金コロイド粒子が入っていますので、抗体陽性の検体でも、Cライン上には常にラインが発生する仕組みになっています。
抗体検査は、このイムノクロマト法を用いた方法で、検体中に抗体があれば、Tライン上で金コロイド粒子がたくさん集まって肉眼で見えるようになるという原理です。
<使用方法>
1) 検体を滴下します。

2) 緩衝液を滴下します。
原理図の左側のサンプルパッドに滴下された血液は、その後に滴下された緩衝液とともに、毛細管現象で右側に移動していきます。途中、抗体は、“新型コロナウイルス抗原の結合した金粒子”に結合しながら右側に移動します。

3) 15分間待ちます。
4) 結果を確認します。
血液中に新型コロナウイルス抗体が存在すれば、金粒子がTライン上に凝集して目で見える線として検出できます。抗体がなければTラインには金粒子が集まらないので、線が出ません。
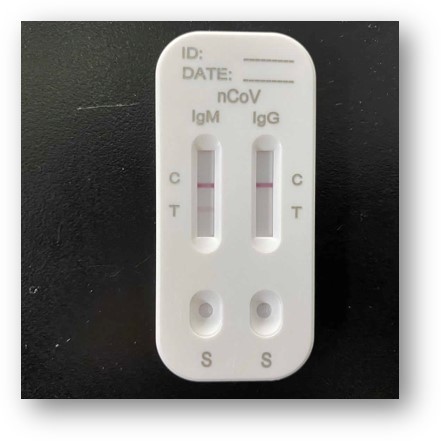
抗体検査の性能と臨床評価
~INNOVITA社の場合~
現在世界中のメーカーが抗体検査を開発を進めており、多数の製品が発売されています。
その中には、臨床的な検証がなされていない製品も含まれているという報道もありますが、INNOVITA社は中国・欧州で診断薬として承認を得ており、さまざまな性能評価が実施されています。※性能評価の詳細はこちらからご確認ください。
抗体検査で重要になる性能は、他の感染症では反応しないという交差反応性の性能です。新型コロナウイルスはこれまでにも多数確認されていて、多くの風邪の原因として知られています。とくにこれら新型コロナウイルスと反応しないことが重要であるといえます。
INNOVITA社の抗体検査は、以下のウイルスIgM抗体、IgG抗体と反応しないことが確認されています。
<IgM抗体>
コロナウイルス HKU1、コロナウイルス OC43、コロナウイルスNL63、コロナウイルス229E、インフルエンザA型 H1N1、インフルエンザA型 H3N2、インフルエンザA型 H5N1、インフルエンザA型 H7N9、インフルエンザB型、RSウイルス、アデノウイルス、ライノウイルス、エンテロウイルスA、EBウイルス、麻疹ウイルス、CMV、水痘・帯状疱疹ウイルス、パラインフルエンザウイルス、肺炎マイコプラズマ、肺炎クラミジア、 コクサッキーBウイルス
<IgG抗体>
コロナウイルス HKU1、コロナウイルス OC43、コロナウイルスNL63、コロナウイルス229E、インフルエンザA型 H1N1、インフルエンザA型 H3N2、インフルエンザA型 H5N1、インフルエンザA型 H7N9、インフルエンザB型、RSウイルス、アデノウイルス、ライノウイルス、エンテロウイルスA、EBウイルス、麻疹ウイルス、CMV、水痘・帯状疱疹ウイルス、パラインフルエンザウイルス、肺炎マイコプラズマ、肺炎クラミジア、 コクサッキーBウイルス
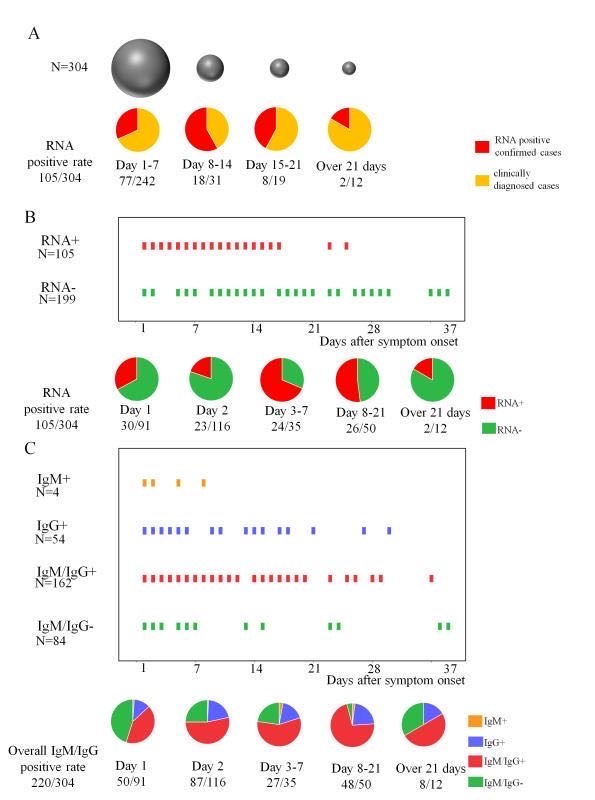
臨床性能も試験済みです。以下の図は、INNOVITA社の臨床性能試験結果です。
この試験では、中国の診断基準にしたがって、CT検査や他の臨床症状で新型肺炎と診断された患者を対象に試験しています。PCR検査と抗体検査の違いがはっきりと分かる結果になっています。
図の上にある円グラフ(A)は、発症日数毎の患者数とPCR検査の陽性率が示されています。赤色が陽性で、オレンジ色が陰性です。臨床症状があっても、PCR陰性となる患者が非常に多いことが示されています。
図の真ん中にある円グラフは、PCR検査の陽性率で、緑色が陰性、赤色が陽性だった患者の割合になります。発症1日目、2日目はPCR陽性率は低いのですが、発症後3-7日になると陽性率は高くなり、その後徐々に陽性率が下がっていきます。
図の一番下にある円グラフは、抗体検査の陽性率で、緑色がIgM抗体もIgG抗体も陰性だった患者、それ以外の色はいずれかの抗体が陽性だった患者の割合です。発症1日目から多くの患者で抗体が検出されています。
つまり、感染初期には、PCR検査は陽性率が約30%でしたが、抗体検査は約60%と、比較的陽性率が高いという解析結果となっています。これは、「抗体検査とPCR検査を同時に実施することで、さらに多くの患者を発見できる」可能性があることを示唆しています。
また、PCR検査との一致率は、以下の表の通りで、感度87.3%、特異度100%という結果が得られています。

このように、INNOVITA社のイムノクロマトキットは、中国国内での試験成績がたくさんあり、臨床現場での使用実績も多数あります。
今回の検証試験では、こういった臨床試験の一部を日本で行うことを想定しています。
抗体検査の使い方と判定方法
~中国では~
新型コロナウイルスの検査や治療は世界中で試験されていますが、中国ではいち早く抗体検査が診断薬として開発され、医療現場で使われています。その使い方はPCR検査を否定するものではなく、お互いが補い合う使われ方です。
<中国での抗体検査の結果判定方法>
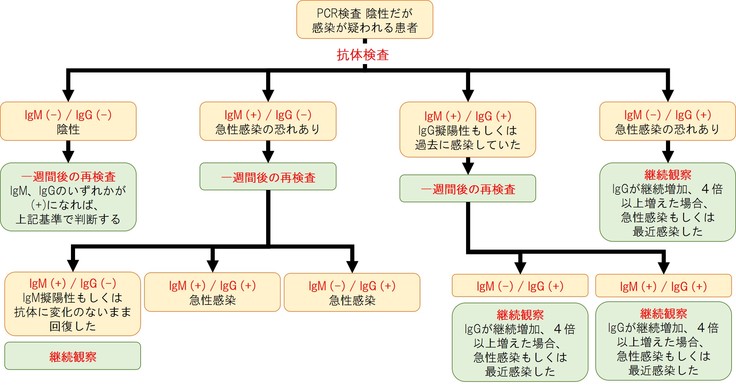
PCR検査は医師の感染リスクが高いうえに、測定にも手間が必要です。日本でも抗体検査を臨床現場で使用できるようにして、医療現場を手助けしたいと考えています。
日本では、少し前から医療崩壊が起こるから検査を増やしてはいけないという論調をよく耳にします。【検査キットが普及する⇒感染者が増える⇒病院が混雑してくる⇒医療資源が足りなくなる⇒医療崩壊】という考え方です。
しかし、医療崩壊の根本原因は、感染者が増えすぎることで、人的資源も含めた医療資源が足りなくなることだと考えます。
検査キットが普及したから感染者が増えるのではないのです。感染者は今この時も増えているかもしれませんが、検査しないと発見できず、感染を広めてしまう可能性があります。
検査キットが普及すると、【感染している患者の早期発見⇒適切な治療(例えば宿泊施設での隔離、自宅待機もしくは入院)】ができ、感染拡大させないというメリットがあるのです。
診断薬化にむけた研究開発フェーズとプロジェクトの位置付け
診断薬を完成するには、3つのフェーズが必要です。
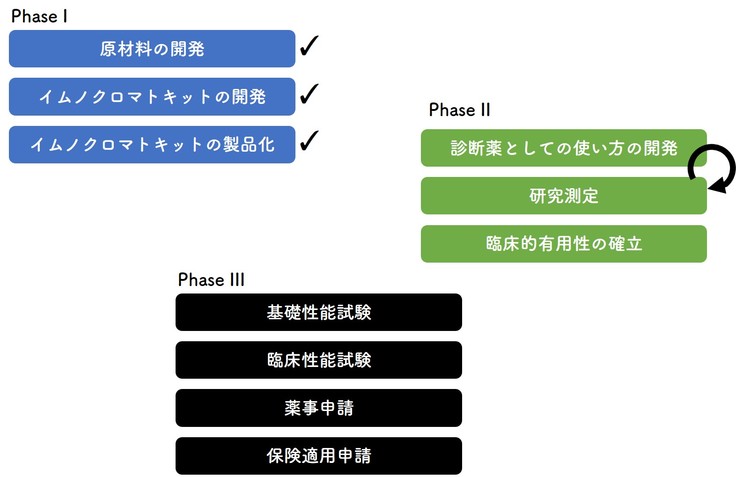
第1フェーズで、抗体検査のイムノクロマトキットを完成させます。第2フェーズでは抗体検査の使用方法やできること・できないことを判明させるための研究測定を行います。これを行うことで、どのような患者に、いつ使用すれば、臨床現場で活用できるのかを明確化していきます。
(第2フェーズは前述の研究スケジュールの①〜③に該当。第3フェーズは④〜⑥に該当。)
もちろん第2フェーズで実施した研究測定の結果、現在完成しているキットの性能が足りていないことが判明する場合もありますので、研究測定の結果、第1フェーズに戻って改良を行う場合もあります。
第2フェーズで診断薬としての使われ方が確定すれば、第3フェーズに移行し、診断薬としての承認を得るための試験を改めて実施していきます。
今回のプロジェクトでは、第2フェーズの「診断薬としての使い方の開発」に関する研究測定を、複数の医療機関と行います。
この抗体検査キットが、日本国内で中国同様の使い方ができるのかどうかを検証していく試験を実施することが目的ですが、まずはこの抗体検査キットが日本国内の患者を検証するに値する性能を持っているのかを検証する試験を計画しています。
まず、日本で感染者と確定した患者のうち、どの程度が抗体を持っているのかのデータが必要です。また、それ以前に現在の日本で抗体陽性者がどの程度いるのかの把握、さらに抗体陽性者が再感染していないかの確認も必要となります。抗体がある=感染しないはまだ証明されていません。
これらには、数千~数万のテストが必要です。今回の試験は、診断薬承認に向けた、入り口です。診断薬として、どのように使っていくのか、そのための方向性を確認するための試験です。
この研究は医療機関様の協力が不可欠です。そういったご協力いただける医療機関様に無償で配布する測定キットの購入資金と、測定にかかる諸経費をぜひ皆様のご協力をよろしくお願いいたします。
正しい診断法を確立するための一歩を
今回のプロジェクトは、いろいろな検査法があって、その中から正しい診断方法を確立していくための一つのステップです。今後、さまざまな診断方法が提案され、検証されていきます。抗体検査の使い方が決まれば、診断薬として必要な性能もはっきりとしてきて、統一した性能基準ができあがり、安心して使用することができるようになっていきます。
今回私たちは新型コロナウイルスが蔓延していき、生活が脅かされていく様を目の当たりにしました。情報も少なく、何をすればいいのか、これからどうなるのかも全く分からない“暗闇”に落とされたような気分になった人も多くいると思います。
でも、医療関係者の皆さんが懸命に最前線で闘ってくれています。ワクチンや治療薬の開発を進めている研究者などもいます。私たちのように診断方法を開発しようと懸命に働いている人もいます。
それぞれの立場で、自分にできることをできる範囲でやっていくことで、新型コロナウイルス感染症を克服し、次に別の感染症が突然蔓延した時に、正しく恐れる社会を作っていけると信じています。
株式会社TKResearch
~研究成果をいち早く臨床現場に~
「研究成果をいち早く臨床現場に」を目指す、体外診断用医薬品の研究開発ベンチャー 株式会社TKReseachです。これまで約20年間にわたって体外診断用医薬品の原材料開発、研究開発、製造、薬事申請を経験した代表が立ち上げたバイオベンチャーで、診断薬の研究開発を業務として行っています。
これまでに数々の診断薬を開発した経験を活かして、Cytometric CBA法(抗横紋筋抗体測定)の共同開発などに成功し、実用化しています。共同開発の活動は、国内だけでなく、中国の医療機器メーカーとも診断薬の共同開発を実施しています。
株式会社TKResearch 代表略歴
代表取締役 稲垣 貴之
東京工業大学 大学院卒業後、様々なメーカーで研究開発に従事し、会社に勤める傍ら、東京大学工学系研究科バイオエンジニアリング専攻で抗体に関する研究で博士(工学)を取得。
抗体を用いた測定系開発や研究開発、製品化研究に従事し、診断薬メーカーにて研究から薬事申請までを統括して、2017年独立。
現在は、診断薬の研究開発を国内外のメーカー・研究機関と共同で実施しながら、コンサルティング・各種講演会を実施している。
●ご留意事項
・このクラウドファンディングは、中国の診断薬メーカー INNOVITA (TANGSHAN) Biological Technology Co.,Ltd. 社が製造する抗体検査キット「COVID-19 IgG/IgMイムノクロマトキット」の日本国内での診断薬承認を目指し、第2フェーズの「診断薬としての使い方の開発」に関する研究測定にかかる費用を集めるものです。
・本製品は研究用試薬です。現時点では、医薬品医療機器法に基づく体外診断薬用医薬品として承認・認証等を受けておらず、日本国内では診断目的では使用できません。また、医療機関向けの販売のため、個人の方等への販売はございません。
・本プロジェクトは、抗体検査キットが診断薬になることを保証するものではありません。診断薬化に向けて必要な研究開発を行い、その結果として再度測定方法の開発が必要になる可能性もあります。
再開発の場合、測定原理自体を変更する必要が出た場合は、開発に1年近くかかる可能性があります。原材料変更等の単純な内容であっても、約半年かかる見込みです。
・研究開発後、法令上の手続きとしては、倫理委員会に申請して試験実施の承認を得る必要があります。倫理委員会は、各医療機関に付属の機関で、定期的に開催されています。万一、開催が遅れるような事態があれば、試験自体も遅れる可能性があります。
・厚生省による診断薬の承認には、通常申請から1年程度の時間を要しますが、国の機関による審査を必要とするプロセスの為、期間を保証するものではありません。承認までの期間は、今後変更や遅れが発生する場合もございます。
以上、ご理解いただけますと幸いです。
・リターンに関する条件の詳細については、「リターンに関するご留意事項」もご確認ください。
あなたのシェアでプロジェクトをさらに応援しよう!
プロフィール
株式会社TKResearch 代表取締役 東京工業大学大学院 生命理工学研究科 バイオテクノロジー専攻 修士課程 東京大学大学院 工学系研究科 バイオエンジニアリング専攻 博士課程 医療機器メーカーで研究所所長として、抗体原材料の研究開発に従事、その後診断薬メーカーにて研究開発~薬事申請までを部長として統括し、2017年独立。 現在は、国内外のメーカーとの共同研究開発や、慶應義塾大学との共同開発成果である「抗横紋筋抗体測定」の受託測定、様々なメーカーのコンサルティング等を手掛けています。
あなたのシェアでプロジェクトをさらに応援しよう!
リターン
5,000円

活動へのご協力
①お礼状の送付(電子メールにて送付)
②進捗報告の活動報告冊子(PDFデータを電子メールにて送付)
*複数口でのご支援も可能です
- 支援者
- 0人
- 在庫数
- 制限なし
- 発送完了予定月
- 2020年10月
10,000円

活動へのご協力
①お礼状の送付(電子メールにて送付)
②進捗報告の活動報告冊子(PDFデータを電子メールにて送付)
③活動報告冊子へのお名前掲載(希望者のみ)
- 支援者
- 7人
- 在庫数
- 制限なし
- 発送完了予定月
- 2020年10月
30,000円

活動へのご協力【ホームページにて感謝をお伝えします】
①お礼状の送付(電子メールにて送付)
②進捗報告の活動報告冊子(冊子郵送)
③活動報告冊子へのお名前掲載(希望者のみ)
④弊社ホームページへのお名前掲載(希望者のみ)
- 支援者
- 0人
- 在庫数
- 制限なし
- 発送完了予定月
- 2020年10月
50,000円

活動へのご協力【ホームページにて感謝をお伝えします】
①お礼状の送付(電子メールにて送付)
②進捗報告の活動報告冊子(冊子郵送)
③活動報告冊子へのお名前掲載(希望者のみ)
④弊社ホームページへのお名前掲載(希望者のみ)
- 支援者
- 1人
- 在庫数
- 制限なし
- 発送完了予定月
- 2020年10月
100,000円

活動へのご協力【ホームページにて感謝をお伝えします】
①お礼状の送付(電子メールにて送付)
②進捗報告の活動報告冊子(冊子郵送)
③活動報告冊子へのお名前掲載(希望者のみ)
④弊社ホームページへのお名前掲載(希望者のみ)
- 支援者
- 1人
- 在庫数
- 制限なし
- 発送完了予定月
- 2020年10月
500,000円

活動へのご協力【感謝のプレートをお送りします】
①お礼状の送付(電子メールにて送付)
②進捗報告の活動報告冊子(冊子郵送)
③活動報告冊子へのお名前掲載(希望者のみ)
④弊社ホームページへのお名前掲載(希望者のみ)
⑤弊社より感謝のプレートをお送りいたします
- 支援者
- 0人
- 在庫数
- 制限なし
- 発送完了予定月
- 2020年10月
プロフィール
株式会社TKResearch 代表取締役 東京工業大学大学院 生命理工学研究科 バイオテクノロジー専攻 修士課程 東京大学大学院 工学系研究科 バイオエンジニアリング専攻 博士課程 医療機器メーカーで研究所所長として、抗体原材料の研究開発に従事、その後診断薬メーカーにて研究開発~薬事申請までを部長として統括し、2017年独立。 現在は、国内外のメーカーとの共同研究開発や、慶應義塾大学との共同開発成果である「抗横紋筋抗体測定」の受託測定、様々なメーカーのコンサルティング等を手掛けています。